 Lukteorgan utforming: lukt og spektroskopi
Lukteorgan utforming: lukt og spektroskopi
av Jonathan Sarfati
Vår luktesans er faktisk et komplekst system utviklet for å oppdage tusenvis av kjemikalier. Det hjelper advare oss mot farer, f.eks råtnende mat-vi kan ane en del av råttent kjøtt, etylmerkaptan, i en konsentrasjon på 1/400 000 000 del av et milligram per liter luft. 1 Lukt hjelper oss også å skille typer matvarer og blomster. Luktesansen er faktisk ansvarlig for det meste av forskjellige "smaker" av matvarer. I mange dyr, er denne forstand enda viktigere enn hos mennesker-det hjelper f. eks. bier finne nektar.
Nesen inneholder millioner av reseptorer, av 500-1000 forskjellige typer. De er i den gule overflatevevet til lukteorganet, som dekker omtrent 2,5 cm2 på hver side av den indre nesen. De ulike typer reseptorer er proteiner, foldet så et spesielt formet lukt-molekyl kan virke. Hver mottaker er koblet til et g-protein. Når lukt molekylet er 'tilkoblet', er g-protein frigitt. Dette utløser en annen budbringer for å stimulere en nervecelle til å sende ut et signal. Dette overføres ved lukteorgan nervefibre som går inn i det ene av to spesialiserte strukturer -lukteorgan pærer (bulbs), som ligger i lagvise projeksjoner under den fremre delen av hjernen. De sortere signalene, og overføre dem til hjernen for behandling. (1,2)
Bilde 1. Neseregionen -med luktesans
Nylig, foreslo Luca Turin, en biofysiker ved University College, London, en mekanisme hvor elektron tunneler fra et donor område til et akseptor nettsted på reseptor molekylet, som forårsaker den til å frigjøre g-protein. Tunnele krever både start og behandling poeng til å ha samme energi, men Turin mener at donorsetet har en høyere energi enn reseptoren. Energien forskjellen er nettopp det som kreves for å opphisse lukt molekyl til en høyere vibrasjons kvantetilstand. Derfor når lukten molekylet lander, kan det absorbere riktig mengde av elektronets energi, slik at tunnel-passering gjennom sine omløpsbaner er mulig. (3)
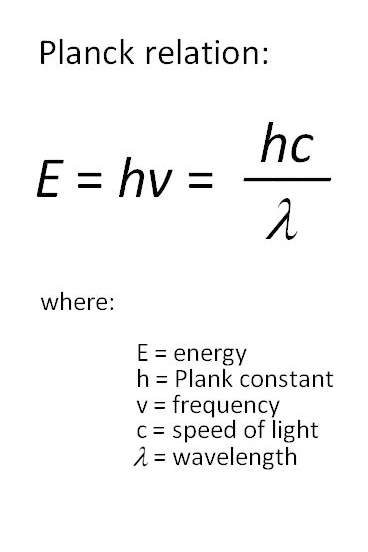 Dette betyr at lukt reseptorene faktisk oppdager energi av vibrasjons kvante-overganger i luktmolekyler, som først foreslått av GM Dyson i 1937. (4)
Dette betyr at lukt reseptorene faktisk oppdager energi av vibrasjons kvante-overganger i luktmolekyler, som først foreslått av GM Dyson i 1937. (4)
Denne energien avtar med økende masse av atomene, og øker med økende bindestyrke. Det avhenger også av symmetrien av molekylet. For en to-atoms molekyl (5) er den grunnleggende overgangs-energi :
E = h / 2 π (k / μ) ½
Der h er Plancks konstant; k er kraft-konstanten til bindingen; og μ er den reduserte masse, som er relatert til massene av de to atomer ved:
μ = m 1 m 2 / (m1+ m 2)
En overgang kan noen ganger være forårsaket av hendelsen elektromagnetisk stråling av riktig frekvens (ν, den greske bokstaven nu). Denne frekvens er relatert til energien ved:
E = h ν
Vibrasjonsspektrum måles normalt i bølgetall (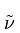 ), den resiproke av bølgelengden, slik at dens enheter er cm-1 (inverse av cm). Bølgetall er relatert til energi ved:
), den resiproke av bølgelengden, slik at dens enheter er cm-1 (inverse av cm). Bølgetall er relatert til energi ved:
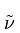 = E / hc
= E / hc
Ettersom denne energi er i det infrarøde området, er infrarød absorpsjonsspektroskopi et vanlig verktøy for å måle vibrasjons energier og bindingsstyrker (sammen med den komplementære teknikken av Raman-spektroskopi).
Dette betyr at visse grupper av atomer har lignende energier, så har også lignende vibrasjonsspektra. For eksempel kjemikalier med svovelhydrogenbindinger tendens til å vibrere på ca 2500 cm -1 og dette blir ofte oppfattet som en "råtten-egg" lukt. Råtne egg produserer kjemikalier som hydrogensulfid (H2S), og etylmerkaptan produsert av råtnende kjøtt er C2H5SH.
Turin støtter sin teori ved å merke seg at kjemiteknikk (B10H14) lukter veldig lik S-H forbindelser, og det har ingenting til felles med dem bortsett fra lignende vibrasjons energier. Selv om bor har en mye lavere atommasse enn svovel, B-H-bindinger er mye svakere enn S-H-bindinger..
Ytterligere støtte ble gitt av den analoge forbindelser ferrocene og nickelocene. Disse har et divalent metall-ion (henholdsvis jern og nikkel) klemt mellom to syklopentadienyl atomer
(C5H5-). Hovedvibrasjons forskjellen mellom dem er at metallring-bånde i ferrocene vibrerer ved 478 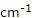 , mens i nickelocene er det 355
, mens i nickelocene er det 355 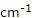 . Ferrocene lukter heller krydret, mens nickelocene lukter lik aromatiske hydrokarbon ringer. Torino foreslår at under en terskel på 400
. Ferrocene lukter heller krydret, mens nickelocene lukter lik aromatiske hydrokarbon ringer. Torino foreslår at under en terskel på 400 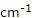 , er vibrasjonssignal belastet av "bakgrunnsstøy", så det ikke oppdages av nesen.
, er vibrasjonssignal belastet av "bakgrunnsstøy", så det ikke oppdages av nesen.
Som forskjellige isotoper har forskjellige masser, men lignende kjemiske egenskaper, påvirker de vibrasjonen energi. Det kan ses fra formelen for redusert masse at den største forskjellen resultatene fra erstatte hydrogen (Ar=1) med deuterium (Ar=2) -der telleren blir fordoblet. Faktisk lukter deuterert acetophenone mer fruktaktig enn vanlig acetophenone (C6H5COCH3). Det lukter også litt av bitre mandler, akkurat som mange forbindelser som inneholder cyanid eller nitril gruppe (C≡N) -både C-D og C≡N obligasjoner vibrerer på ca 2200 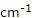 .
.
En utfordring til Turins teori er de forskjellige lukter av noen optiske isomerer, som har identiske vibrasjonsspektra. For eksempel, lukter R-carvone som peppermynte, og S-carvone som karve. Svaret er: spektrene er identiske bare i symmetriske medier, som i oppløsning eller i gassfase. Men lukten av reseptorene er i molekylpar og orientere de to strukturstoffene forskjellig. Dette betyr at forskjellige vibrerende grupper ligger i tunnelretningen for hver optiske isomer. Turin mener at karve S-karvon er orientert slik at en karbonylgruppe
(C = O) gruppe ligger i en retning, så den blir detektert; i minte R-karvon, ligger den i rett vinkel, så der blir den ignorert. Turin støttet denne ved fremstilling av en karve duft ved å blande minte-karvon med den karbonyl-inneholdende butanon (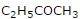 ).
).
Hvis Turins teori er sann, så ville infrarød og Raman-spektroskopi være viktige verktøy for parfyme industrien! Turin er også å bruke uelastisk tunnell spektroskopi -'inelastic 'refererer til energitap før tunnel gjennomgang, som med den foreslåtte sensoriske mekanismen.
Den nøyaktige kjemien for luktesansen er fortsatt lite forstått. Men Turin mener han har funnet en sekvens av aminosyrerester, som kan fungere som elektrondonor sammen med NADPH. Han har også funnet fem rester koordinert til et sinkatom som kan være mottakerstedet. En advarsel tegn på sinkmangel er tap av luktesans, og sink er ofte involvert i biologiske elektron-overføringsreaksjoner.
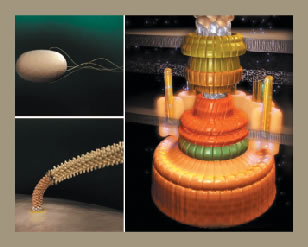 Uansett om Turins idé er riktig eller ikke, viser luktsystemet hva biokjemiker Michael Behe kaller irreduserbar kompleksitet, og er derfor bevis på design (6). Dette betyr at systemet krever mange deler for at det skal fungere, og vil ikke fungere hvis noen manglet. Kjemisk sansings maskineri trenger proteiner med akkurat den rette form for å innlosjere luktmolekylene. Og under Turins-modell, de riktige energinivåene også. Og selv om sensorene var i full drift, vil den kjemiske informasjonen som samles inn av nesen være ubrukelig uten nerveforbindelsene for å sende dem, og hjernen til å behandle dem.
Uansett om Turins idé er riktig eller ikke, viser luktsystemet hva biokjemiker Michael Behe kaller irreduserbar kompleksitet, og er derfor bevis på design (6). Dette betyr at systemet krever mange deler for at det skal fungere, og vil ikke fungere hvis noen manglet. Kjemisk sansings maskineri trenger proteiner med akkurat den rette form for å innlosjere luktmolekylene. Og under Turins-modell, de riktige energinivåene også. Og selv om sensorene var i full drift, vil den kjemiske informasjonen som samles inn av nesen være ubrukelig uten nerveforbindelsene for å sende dem, og hjernen til å behandle dem.
Bilde Y. Skal bakterie-flagell fungere -må den være komplett
Referanser:
1. Sensory reception: smell (olfactory) sense. Britannica CD, Version 97. Encyclopædia Britannica, Inc. 1997. Return to text
2. Hill, S., 1998. Sniff’n’shake. New Scientist 157(2115):34-37. Return to text
3. Turin, L., 1996. A spectroscopic mechanism for primary olfactory reception. Chemical Senses 21:773-791 | doi:10.1093/chemse/21.6.773.
4. Sell, C., 1997. On the right scent. Chemistry in Britain, 33(3):39-42. Return to text
5. For more complicated molecules, see Wilson, E.B., Decius, J.C. and Cross, P.C., 1955. Molecular Vibrations: the Theory of Infrared and Raman vibrational spectra, McGraw-Hill, New York. Return to text
6. Behe, M. J., 1996. Darwin’s Black Box: The Biochemical Challenge to Evolution, The Free Press, New York.
Stoffutvalg og bilder ved Asbjørn E. Lund
 Lukteorgan utforming: lukt og spektroskopi
Lukteorgan utforming: lukt og spektroskopi Lukteorgan utforming: lukt og spektroskopi
Lukteorgan utforming: lukt og spektroskopi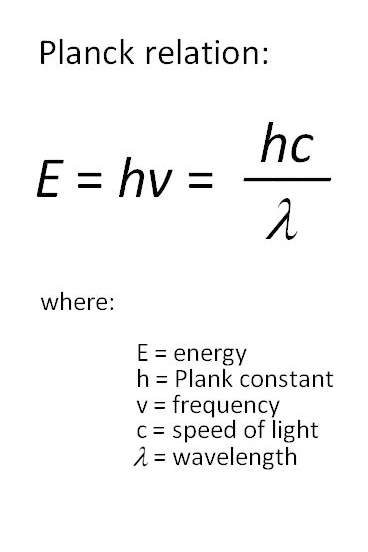 Dette betyr at lukt reseptorene faktisk oppdager energi av vibrasjons kvante-overganger i luktmolekyler, som først foreslått av GM Dyson i 1937. (4)
Dette betyr at lukt reseptorene faktisk oppdager energi av vibrasjons kvante-overganger i luktmolekyler, som først foreslått av GM Dyson i 1937. (4) Uansett om Turins idé er riktig eller ikke, viser luktsystemet hva biokjemiker Michael Behe kaller irreduserbar kompleksitet, og er derfor bevis på design (6). Dette betyr at systemet krever mange deler for at det skal fungere, og vil ikke fungere hvis noen manglet. Kjemisk sansings maskineri trenger proteiner med akkurat den rette form for å innlosjere luktmolekylene. Og under Turins-modell, de riktige energinivåene også. Og selv om sensorene var i full drift, vil den kjemiske informasjonen som samles inn av nesen være ubrukelig uten nerveforbindelsene for å sende dem, og hjernen til å behandle dem.
Uansett om Turins idé er riktig eller ikke, viser luktsystemet hva biokjemiker Michael Behe kaller irreduserbar kompleksitet, og er derfor bevis på design (6). Dette betyr at systemet krever mange deler for at det skal fungere, og vil ikke fungere hvis noen manglet. Kjemisk sansings maskineri trenger proteiner med akkurat den rette form for å innlosjere luktmolekylene. Og under Turins-modell, de riktige energinivåene også. Og selv om sensorene var i full drift, vil den kjemiske informasjonen som samles inn av nesen være ubrukelig uten nerveforbindelsene for å sende dem, og hjernen til å behandle dem.